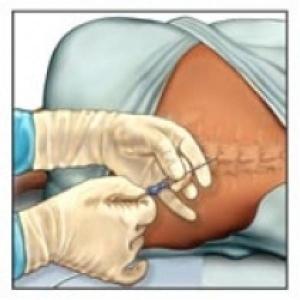
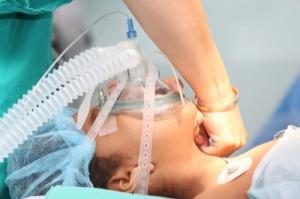
Предыдущая глава Глава 3 Следующая глава
ГЛАВА 3. Гемодинамика больных в операционном и послеоперационном периодах в условиях стресспротекторной терапии
Содержание 3-й главы:
3.1.1. Изменение трендов артериального давления и ЧСС
3.1.2. Изменение основных параметров системной гемодинамики
3.1.3. Изменение показателей сердечного ритма
3.2.1. Изменение параметров мозгового кровотока
3.2.2. Изменение параметров печеночного кровотока
3.3.1. Изменение параметров гемодинамики и микроциркуляции у больных с исходной артериальной нормотонией
3.3.2. Изменение центральной гемодинамики и микроциркуляции у больных с исходной артериальной гипотонией
3.3.3. Изменение центральной гемодинамики и микроциркуляции у больных с исходной артериальной гипертензией
3.4.1. Изменение центральной гeмодинамики
3.4.2. Изменение показателей объемного пульса
3.5.1. Изменение ОЦК и показателей красной крови у больных с исходной нормоволемией
3.5.2. Изменение ОЦК, и показателей красной крови у больных с исходной гиповолемией
В начало 3-й главы К содержанию монографии
3.1. Изменение основных показателей системной гемодинамики у больных в операционном периоде при проведении лапароскопических холецистэктомий на фоне стресспротекции клофелином.
Кровообращению, с момента открытия В. Гарвеем в 1615 году, как жизненно важной функции организма постоянно придается большое значение, тем более что гемодинамические сдвиги считают наиболее значимыми негативными эффектами при лапароскопических холецистэктомиях (B. Fagher, J. Magn Нusson, 1994; U. Windberger, H. Siegl, 1994; W.A. Loder, 1994), в связи с чем повышается потенциальный риск системных нарушений (A.P. Sobolewski, R.M. Deshmukh, B.L. Brunson, 1995; H.R. Munoz, C.M. Sacco, 1997; R. Stuttmann, C. Vogt, E. Eypasch, M. Doehn, 1995; J.B. Nyarwaya, J.X. Mazoit, 1994; М.Г. Лепилин, 1987; K. Isaaz, J.F. Bruntz, 1994).
В начало 3-й главы К содержанию монографии
3.1.1. Изменение трендов артериального давления и ЧСС
В клинической практике, с позиции практического анестезиолога, следует учитывать важность значения рутинных параметров мониторирования — гемодинамических трендов систолического и диастолического артериального давления, ЧСС.
В контрольной группе (табл. 3.1, рис. 3.1) в день операции, до премедикации, отмечаются незначительное повышение АДс на 2,1 %, АДд на 0,4 % относительно исходных значений. После проведения премедикации и поступления в операционную отмечалось достоверное повышение АДс на 4,6 % при недостоверном увеличении АДд на 3 %, что несомненно является проявлением стрессреакции на предстоящее вмешательство. Наблюдается последующее снижение (возврат к исходным значениям) АДс при недостоверном увеличении АДд (на 2,1 %) после индукции. Интубация трахеи вызывала достоверное повышение АДс на 4,9 % относительно исходных значений. После инсуффляции углекислого газа в брюшную полость отмечается снижение АДс на 5,2 %. Достоверное снижение АДс происходило также на этапах выделения и работы на тубулярных структурах, холецистэктомии – на 9,6 % и 7,2 % соответственно. Изменение АДс происходило при небольших изменениях АДд, достоверное снижение на 4,8 % отмечается лишь на этапе выделения желчного пузыря и работы на тубулярных структурах. После снятия искусственного пневмоперитонеума (ИПП) и после операции показатели артериального давления возвращались к исходным значениям, недостоверно снижаясь в послеоперационном периоде.
Приведенные выше данные свидетельствуют, что у больных контрольной группы наблюдаются значимые изменения показателей артериального давления, которые являются следствием воздействия на организм пациента стрессовых и иных неблагоприятных факторов, действующих на организм пациента до и во время вмешательства.
Таблица 3.1.
Изменение основных гемодинамических трендов АДс, АДд и ЧСС в контрольной и исследуемой группах (M m, * – p<0.05 – по сравнению с первым этапом).
|
Показа-тель |
Исх. |
Дооп. |
Прем. |
Инд. |
Инт. |
Инсф. |
Выд. |
Хэкт. |
Кон. |
Пер. |
Попр. |
|
АДс К (мм.рт.ст.) |
136,0 |
138,9 |
142,3 |
135,7 |
142,6 |
128,9 |
122,9 |
126,2 |
134,6 |
136,7 |
132,7 |
|
± 1,5 |
± 1,9 |
± 2,0* |
± 2,3 |
± 2,8* |
± 2,3* |
± 2,2* |
± 2,0* |
± 2,0 |
± 1,9 |
± 1,8 |
|
|
И |
137,6 |
140,6 |
137,6 |
132,7 |
140,0 |
126,9 |
121,5 |
126,7 |
134,5 |
135,6 |
132,4 |
|
± 2,4 |
± 2,8 |
± 2,1 |
± 3,0 |
± 2,2 |
± 2,1* |
± 1,9* |
± 1,8* |
± 1,8 |
± 1,7 |
± 1,6 |
|
|
АДд К (мм.рт.ст.) |
84,7 |
85,0 |
87,2 |
86,5 |
88,9 |
82,4 |
80,6 |
83,7 |
86,3 |
86,8 |
84,1 |
|
± 1,3 |
± 1,4 |
± 1,7 |
± 1,6 |
± 1,9 |
± 1,5 |
± 1,5* |
± 1,3 |
± 1,3 |
± 1,1 |
± 0,9 |
|
|
И |
84,3 |
84,6 |
84,7 |
84,8 |
87,3 |
83,0 |
80,3 |
82,1 |
85,2 |
85,6 |
84,8 |
|
± 1,5 |
± 1,4 |
± 1,4 |
± 1,2 |
± 1,0 |
± 1,1 |
± 1,1* |
± 1,1 |
± 1,0 |
± 1,0 |
± 0,9 |
|
|
ЧСС К (уд/мин) |
78,7 |
80,2 |
90,2 |
94,5 |
96,7 |
93,1 |
92,9 |
93,9 |
90,3 |
90,1 |
85,6 |
|
± 0,8 |
± 1,0 |
± 1,4* |
± 1,6* |
± 1,5* |
± 1,6* |
± 1,3* |
± 1,1* |
± 1,3* |
± 1,3* |
± 1,2* |
|
|
И |
79,5 |
80,8 |
86,0 |
90,4 |
92,4 |
89,7 |
89,6 |
89,8 |
86,3 |
86,1 |
85,1 |
|
± 0,9 |
± 1,3 |
± 1,2* |
± 1,4* |
± 1,3* |
± 1,3* |
± 1,3* |
± 1,3* |
± 1,2* |
± 1,2* |
± 1,2* |

Рисунок 3.1. Изменение АДс и АДд в контрольной и исследуемой группах
Наиболее значимые изменения в контрольной группе происходили на этапах интубации, где отмечается повышение показателей артериального давления, сопровождающееся увеличением ЧСС, и инсуффляции, где отмечается снижение показателей артериального давления, причем без существенного изменения ЧСС (по сравнению с предыдущим этапом). После снятия ИПП наблюдается восстановление (возрастание – в данном случае) показателей артериального давления, сопоставимое с их дооперационным уровнем.
В исследуемой группе, на фоне стресспротекции клофелином (табл. 3.1, рис. 3.1) показатели артериального давления остаются неизменными на всех этапах, исключая этапы инсуффляции, выделения и холецистэктомии. Незначительное повышение на 2,2 % в день операции на дооперационном этапе АДс не является достоверным, после премедикации АДс остается стабильным, равным исходным значениям. Снижение на 3,6 % после индукции не является достоверным, также как и незначительное повышение на 1,7 % после интубации. После достоверного снижения АДс на этапах инсуффляции, выделения и холецистэктомии (соответственно 7,8 %, 11,7 %, 7,9 %), происходит возврат к исходным значениям (недостоверно ниже на 2.3 %). Артериальное давление остается неизменным при переводе и в послеоперационном периоде (АДс недостоверно ниже исходных значений на 1,4 % и 3,8 % соответственно).
Диастолическое давление не подвержено значимым изменениям практически на всех этапах исследования, кроме выделения, – отмечается достоверное снижение на 4,7 % относительно исходных значений АДд до 80,3 мм.рт.ст. В целом предел колебаний АДд составляет от 82,1 мм.рт.ст. на этапе холецистэктомия до 87,3 мм.рт.ст на этапе интубация, процент изменения на указанных этапах от – 2,6 % и до + 3.6 %.
Отмечается достоверное снижение диастолического артериального давления (АДд) на 4,7 % на этапе выделения в исследуемой группе, что, однако, не является признаком гипотензии (АДд – 80,3 мм.рт.ст в среднем по группе на данном этапе при АДс – 121,5 мм.рт.ст), не сопровождалось выраженной тахикардией (ЧСС – 89,6) и иными неблагоприятными системными нарушениями и клиническими проявлениями.
После поступления в операционную, после премедикации в исследуемой группе наблюдается повышение ЧСС на 8,1 %, после индукции на 13,6 %, после интубации на 16,2 %. На последующих этапах – инсуффляция, выделение и холецистэктомия – колебания ЧСС незначительны относительно предыдущих этапов операции, составляют от 12,6 % до 12,8 %. ЧСС выше исходного уровня в конце операции на 8,5 % относительно исходных значений, на 7,0 % в послеоперационном периоде.
Следует отметить, что показатели артериального давления, как в контрольной, так и в исследуемой группе, в среднем были в пределах допустимых норм, не отмечено снижения показателей артериального давления ниже допустимых границ. Также не отмечено проявлений артериальной гипертензии. Изменения показателей артериального давления свидетельствуют о приспособлении организма к новым условиям существования в условиях проводимого вмешательства. Наблюдались отдельные случаи исходной артериальной гипертензии как в контрольной (4), так и в исследуемой группах (6), что, видимо, следует связывать с особенностями реакции организма на действующие стресс-факторы, с индивидуальными свойствами сердечно-сосудистой системы.
Изменения показателей артериального давления и ЧСС на этапах исследования свидетельствуют о значимых изменениях в организме пациентов в ответ на проводимое вмешательство. В то же время, используемые анестезиологические схемы и операционные условия в обеих группах не приводят к критическим изменениям артериального давления, выраженной тахи- и брадикардии, артериальной гипо- и гипертензии. Следует сказать, что изменения в исследуемой группе, где проводилась дополнительная защита клофелином, были менее выраженными, а на многих этапах и вообще несущественными, компенсаторного характера.
Показатели артериального давления являются важными параметрами, постоянный мониторинг которых позволяет определить изменения в организме пациента, происходящие в ответ на проводимое вмешательство, оценить эффективность анестезии, проводимой медикаментозной защиты. Но вместе с тем, они, являясь производными показателями (зависимыми от минутного объема сердца, общей резистентности сосудистого русла, состояния волемии, вязкости крови и некоторых других), не характеризуют в полной мере состояние системной гемодинамики. Для изучения характера происходящих изменений нами проведено исследование основных показателей системной гемодинамики.
В начало 3-й главы К содержанию монографии
3.1.2. Изменение основных параметров системной гемодинамики
В контрольной группе (табл. 3.2, рис. 3.2) при поступлении в операционную, после премедикации отмечается достоверное повышение САД на 6,1 %. Также отмечается повышение САД относительно исходных значений на 9,7 % после интубации. После инсуффляции отмечается снижение значений САД до исходного уровня, с незначительным снижением на 0,8 % на этапе холецистэктомии. Недостоверное увеличение на 2,7 % средних значений САД в конце операции позволяет говорить о восстановлении дооперационного уровня САД.
Таблица 3.2.
Изменение основных показателей системной гемодинамики в контрольной и исследуемой группах (M m, * – p<0.05 – по сравнению с первым этапом).
|
Этап |
САД |
ЧСС |
УО |
УИ |
МОС |
СИ |
ОПС |
ПМО2 |
МРЛЖ |
|
Исх . К |
100,3 |
80,4 |
63,9 |
35,8 |
5129,0 |
2877,0 |
1621,4 |
10654,1 |
6999,9 |
|
± 1,9 |
± 1,2 |
± 2,4 |
± 1,4 |
± 202,4 |
± 116,9 |
± 72,4 |
± 239,9 |
± 305,7 |
|
|
И |
99,9 |
79,1 |
64,3 |
36,4 |
5054,2 |
2861,9 |
1614,6 |
10447,3 |
6844,4 |
|
± 2,3 |
± 1,4 |
± 1,8 |
± 1,0 |
± 132,5 |
± 78,8 |
± 65,5 |
± 282,9 |
± 209,7 |
|
|
Прем. К |
106,4 |
93,0 |
53,5 |
30,0 |
4928,2 |
2759,2 |
1792,7 |
13296,8 |
7167,3 |
|
± 2,2* |
± 2,0* |
± 2,5* |
± 1,4* |
± 211,6 |
± 117,2 |
± 74,9 |
± 325,0* |
± 361,5 |
|
|
И |
99,7 |
85,2 |
59,6 |
33,8 |
5051,3 |
2864,9 |
1620,5 |
11153,5 |
6851,7 |
|
± 2,0 |
± 1,3* |
± 2,2 |
± 1,3 |
± 170,4 |
± 104,3 |
± 64,2 |
± 271,7 |
± 278,5 |
|
|
Инт. К |
110,0 |
102,0 |
45,1 |
25,2 |
4587,3 |
2561,4 |
1976,0 |
14746,9 |
6882,5 |
|
± 2,8* |
± 1,7* |
± 1,7* |
± 0,9* |
± 179,7* |
± 90,9* |
± 80,7* |
± 417,4* |
± 323,0 |
|
|
И |
101,1 |
94,1 |
54,5 |
31,0 |
5105,9 |
2901,1 |
1651,7 |
12551,7 |
7029,8 |
|
± 1,9 |
± 1,5* |
± 2,4* |
± 1,5* |
± 221,5 |
± 136,6 |
± 78,3 |
± 299,7* |
± 360,0 |
|
|
Инсф. К |
100,7 |
99,7 |
42,1 |
23,6 |
4171,7 |
2332,8 |
2018,8 |
13050,5 |
5775,9 |
|
± 2,2 |
± 1,9* |
± 2,1* |
± 1,1* |
± 196,2* |
± 106,7* |
± 91,1* |
± 370,3* |
± 339,7* |
|
|
И |
96,1 |
90,9 |
52,8 |
29,9 |
4767,7 |
2701,5 |
1705,3 |
11227,0 |
6223,8 |
|
± 1,9 |
± 1,6* |
± 2,5* |
± 1,5* |
± 215,7 |
± 125,4 |
± 102,4 |
± 271,1 |
± 309,8 |
|
|
Хэкт. К |
99,5 |
98,1 |
42,7 |
23,9 |
4158,6 |
2323,0 |
2017,6 |
12493,0 |
5689,9 |
|
± 1,9 |
± 1,7* |
± 2,4* |
± 1,3* |
± 221,8* |
± 118,3* |
± 93,9* |
± 298,5* |
± 364,7* |
|
|
И |
93,8 |
90,1 |
52,9 |
29,9 |
4759,7 |
2695,3 |
1650,0 |
11005,8 |
6059,0 |
|
± 1,4* |
± 1,3* |
± 2,2* |
± 1,3* |
± 206,8 |
± 120,7 |
± 78,5 |
± 210,8 |
± 260,6 |
|
|
Кон. К |
102,9 |
97,7 |
44,6 |
25,0 |
4301,6 |
2407,0 |
1993,3 |
13081,9 |
6061,3 |
|
± 2,0 |
± 1,8* |
± 2,2* |
± 1,3* |
± 183,7* |
± 102,9* |
± 91,8* |
± 328,3* |
± 312,6* |
|
|
И |
98,1 |
85,8 |
54,5 |
30,9 |
4663,3 |
2640,8 |
1727,9 |
11102,8 |
6211,0 |
|
± 1,5 |
± 1,4* |
± 1,8* |
± 1,1* |
± 154,6 |
± 91,3 |
± 67,1 |
± 269,2 |
± 217,4* |
В результате стрессорного воздействия происходит достоверное увеличение ЧСС на всех этапах исследования, причем максимальное увеличение отмечается после интубации трахеи – на 26,9 % от исходного уровня. На других этапах исследования ЧСС также увеличивается значимо – от 15,6 % после премедикации, до 24,0 % после инсуффляции. После операции ЧСС также выше исходных значений на 21,6 %.
Одновременно с увеличением ЧСС происходит снижение УО. После премедикации УО снижается на 16,3 % от исходных значений, после интубации – на 29,5 %, после инсуффляции, создания ИПП снижение УО отмечается на 34,1 %, а после холецистэктомии до 33,1 %. После операции УО в контрольной группе ниже исходного уровня на 30,3 %.
Изменения УИ были идентичными колебаниям УО, значимо снижаясь уже после поступления в операционную (на 16,3 %). Значения УИ остаются ниже исходного уровня во время (ниже от 29,7 % до 33,1 %) и после операции (30,3 %).
МОС существенно не изменяется после поступления в операционную, недостоверно снижаясь на 3,9 %. Но после интубации происходит достоверное снижение МОС на 10,6 %. Еще более значимое снижение МОС происходит после инсуффляции – на 18,7 %. Оставаясь на этом значении, МОС практически не изменяется на этапе холецистэктомии (ниже на 18,9 %), оставаясь достоверно ниже исходных значений на 16,1 % и после операции.
Изменения СИ, как и МОС, также происходят в сторону уменьшения относительно исходного уровня. Уменьшение на 11,0 % происходит на этапе интубации, в последующем снижение на 18,9 % – на этапе инсуффляции, на 19,3 % – на этапе холецистэктомии и на 16,3 % – после операции. Все это говорит о существенном угнетении сердечного выброса, происходящем, несмотря на возрастание ЧСС, под воздействием ЛХ и других стрессогенных факторов.
После премедикации ОПС остается неизменным, недостоверно повышаясь на 10,6 %, но наблюдается повышение его на последующих этапах. После интубации ОПС достоверно возрастает на 21,9 %, остается повышенным на этапах инсуффляции и холецистэктомии (24,5 % и 24,4 % соответственно). Не отмечается значимого снижения ОПС и после операции(выше исходного значения на 22,9 %).
Потребность миокарда в кислороде в результате воздействия на организм стрессфакторов увеличивается. Отмечается возрастание ПМО2 на 24,8 % после премедикации, на 38,4 % после интубации. После инсуффляции ПМО2 снижается, но остается достоверно выше исходного уровня на 22,5 %. На этапе холецистэктомии ПМО2 выше на 17,3 %, после операции – на 22,8 %.
Показатель МРЛЖ достоверно снижается после инсуффляции на 17,5 %, не изменяется далее на этапе холецистэктомии – ниже исходного на 18,7 %, несколько возрастает после операции – отмечается снижение на 13,4 % относительно исходных значений. Уменьшение МРЛЖ, очевидно, было связано с угнетением ударного объема и сердечного выброса. Анализируя в целом характер изменений показателей системной гемодинамики в контрольной группе, следует отметить, что наиболее значимые изменения происходят на этапах интубации трахеи, выделения. Кроме того, наибольшая стрессорная перестройка системного кровообращения с существенным изменением основных параметров СГД происходит на этапе интубации трахеи. Именно здесь происходит первое значимое стресс-воздействие на организм, мобилизующее защитные силы и требующее адекватной защиты.

Рисунок 3.2. Изменение САД, УО и УИ в контрольной и исследуемой группах
После инсуффляции наблюдаются негативные изменения в гемодинамической картине, говорящие о происходящем уменьшении сердечного выброса вследствие создания ИПП и воздействия ЛХ. Возрастание ОПС свидетельствует о затратном, нерациональном гемодинамическом режиме, что на фоне стрессорной активации и воздействия иных неблагоприятных факторов создает предпосылки для нарушения системного кровообращения. Возрастание действия стресс-факторов на травматичном этапе – холецистэктомии – еще более усугубляет эту ситуацию.
В исследуемой группе с клофелином (табл. 3.2, рис. 3.2) изменение параметров системной гемодинамики было менее значимым в количественном и качественном отношении.
После поступления в операционную, после премедикации и после интубации в этой группе не отмечается значимого изменения САД. Недостоверное снижение на 3,9 % относительно исходных значений происходит после инсуффляции. Достоверное снижение на 6,1 % отмечается на этапе холецистэктомии, в условиях имеющегося ИПП, но в допустимых пределах – 93,8 мм.рт.ст. После десуффляции отмечается восстановление дооперационного уровня САД.
Возрастание ЧСС вследствие стрессорных воздействий и использования атропина отмечается на всех этапах, увеличиваясь на 7,7 % после премедикации. На этапе интубации увеличение происходит на 19,0 %, на этапе инсуффляции – на 14,9 %, холецистэктомии – на 13,9 %. В конце операции ЧСС выше исходного уровня на 8,5 %.
После поступления в операционную в исследуемой группе наблюдается стабильность значений УО и УИ на исходном уровне. Последующая интубация снижала УО на 15,2 %, УИ на 14,9 %. После инсуффляции не происходило дальнейшего снижения УО и УИ, значения УО были ниже исходного уровня на 17,8 %, УИ на 17,7 %, оставаясь неизменными на этапе холецистэктомии. После операции происходило некоторое увеличение УО до 15,2 % и УИ до 15,1 % по сравнению с предыдущим этапом.
Предел изменений МОС на этапах исследования был незначительным. Отмечается недостоверное возрастание на 1,0 % после интубации, недостоверное снижение на 7,7 % после операции. Недостоверные изменения СИ позволяют говорить о стабильности показателей МОС и СИ в исследумой группе, при использовании премедикации с дополнительной нейровегетативной защитой клофелином.
Также не отмечается значимых изменений ОПС, хотя в целом отмечается некоторая тенденция к недостоверному увеличению с 0,4 % после интубации до 7,0 % после операции.
Отмечается возрастание на 20,1 % ПМО2 на этапе после интубации, достоверно увеличение ПМО2 на этапах холецистэктомии и после операции (на 5,3 % и 6,3 % соответственно).
Наблюдается достоверное снижение МРЛЖ на этапе холецистэктомии на 11,5 %, после операции на 9,3 %.
В сравнении с контрольной группой, изменение показателей в исследуемой группе было менее выраженным. Характер изменений показателей системной гемодинамики в исследуемой группе говорит, что наибольшие изменения происходят на этапе инсуффляции, что следует связывать с созданием ИПП. Однако, при этом стрессорный характер изменений в исследуемой группе не так выражен, как в контрольной. В частности, уменьшение УО и УИ происходит в меньшей степени, незначительное изменение МОС и СИ происходит в пределах, позволяющих говорить о стабильности этих параметров. Также наблюдается меньшее увеличение ЧСС, не отмечается увеличения ОПС, то есть изменение гемодинамической ситуации происходит при вполне удовлетворительных условиях, носит компенсаторный характер.
В начало 3-й главы К содержанию монографии
3.1.3. Изменение показателей сердечного ритма
Сердечный ритм, являясь важной характеристикой, зависит от многих воздействий. Изменения сердечного ритма зависят от степени стрессорного воздействия, непосредственно характеризуя состояние регуляторных систем, преобладание активности различных отделов вегетативной нервной системы, и, в том числе, конечно, и состояние самого сердца как органа.
При статистическом анализе сердечного ритма, предложенного Р.М. Баевским, можно выявить числовые параметры, характеризующие составлящие ритма. Математический анализ кардиоинтервалограмм позволяет оценить состояние напряженности различных отделов вегетативной нервной системы (Р.М. Баевский, 1984).
Нами исследовались показатели амплитуда моды (АМо) и индекс напряжения (ИН), характеризующие состояние и взаимодействие отделов вегетативной нервной системы.
В контрольной группе (табл. 3.3) после премедикации АМо не изменяется, после интубации повышается на 6,1 %. Снижение ИН после премедикации на 21,8 % (достоверный сдвиг), после интубации снижение на 16,3 %, но не подтвержденное статистически.
Таблица 3.3.
Изменение показателей ритма сердца (АМо, ИН) в контрольной и исследуемой группах (M m, * – p<0.05 – по сравнению с первым этапом)
|
Показатель |
Исходное |
Премедикация |
Интубация |
|
АМо К |
72,40 |
69,60 |
76,80 |
|
± 1,21 |
± 4,26 |
± 2,15 |
|
|
И |
73,20 |
59,40 |
59,00 |
|
± 2,06 |
± 4,28* |
± 4,00* |
|
|
ИН К |
750,00 |
586,40 |
628,00 |
|
± 40,74 |
± 15,20* |
± 54,90 |
|
|
И |
732,00 |
324,00 |
266,00 |
|
± 39,29 |
± 36,96* |
± 28,91* |
В исследуемой группе (табл. 3.3) после премедикации происходит снижение АМо на 18,9 %, после интубации на 19,4 %. Снижение ИН после премедикации – на 55,7 %, после интубации – на 63,7 %. Следует отметить достоверность изменений в исследуемой группе.
Снижение АМо и ИН в исследуемой группе свидетельствует о меньшей напряженности регуляторных систем за счет снижения тонуса симпатической части вегетативной нервной системы при использовании клофелина в качестве средства для дополнительной защиты.
Таким образом, включение клофелина в премедикацию с целью создания дополнительной антистрессорной защиты позволило уменьшить стрессорную перестройку основных гемодинамических трендов АД и ЧСС, что выражалось в меньшем возрастании АДс и АДд, ЧСС при поступлении в операционную, в ответ на ларингоскопию и интубацию трахеи, на этапах операции и в ближайшем послеоперационном периоде. Снижение АД, происходящее при создании ИПП, отмечается в обеих группах, при использовании клофелина не отмечается возникновения гипотонии, депрессии показателей системной гемодинамики.
В ответ на проводимое вмешательство отмечается изменение показателей системной гемодинамики в обеих группах. В исследуемой группе наблюдаются более стабильные значения ударного и сердечного выбросов при меньшем компенсаторном возрастании ЧСС и при отсутствии возрастания ОПС. В контрольной группе изменения носят стрессовый характер, несмотря на возрастание ЧСС и ОПС, происходит снижение МОС при уменьшении УО. Отмечается возрастание ПМО2 и снижение эффективной работы, что выражается в снижении МРЛЖ.
Дополнительная защита клофелином позволила уменьшить стрессорное воздействие на организм, что проявлялось снижением на этапах исследования показателей математического анализа кардиоинтервалограммы – ИН и АМо.
Включение клофелина в премедикацию позволяет проводить эффективную анестезиологическую защиту организма от неблагоприятных воздействий, в достаточной мере адаптирует системные гемодинамические функции к требованиям операционного стресса.
В начало 3-й главы К содержанию монографии
3.2. Изменение параметров регионального кровообращения у больных в операционном периоде на фоне антистрессорной защиты клофелином
3.2.1. Изменение параметров мозгового кровотока
Исследование показателей мозгового кровотока проводили методом реоэнцефалографии (Х.Х. Яруллин, 1984; М.К. Осколкова, Г.А. Красина, 1980) по стандартной методике с билатеральным расположением электродов.
Контрольную группу составили 25 пациентов, у которых в премедикацию включали стандартную схему: атропин, промедол, димедрол. Исследуемую группу составили 25 пациентов, у которых в премедикацию включали схему: атропин, промедол, димедрол и клофелин.
Указанные показатели исследовали на этапах:
- исходный, за сутки до операции, в палате;
- после премедикации на столе, до операции и индукции;
- после интубации, до начала операции;
- после инсуффляции, до начала работы на тубулярных структурах и выделения желчного пузыря;
- холецистэктомия, после проведения холецистэктомии;
- конец операции, после снятия пневмоперитонеума.
В контрольной группе (табл. 3.4, рис. 3.3) после премедикации отмечается незначительное недостоверное снижение РИ. После интубации и вводного наркоза снижение РИ более значимо и ниже исходных значений на 22,3 %. После инсуффляции также отмечается снижение РИ на 28,6 % от исходного уровня, еще более выраженное в сравнении с первым этапом исследования, что позволяет говорить об имеющемся изменении кровотока в указанном регионе после создания ИПП. РИ также остается ниже исходного и на этапе холецистэктомии. После операции отмечается возрастание РИ относительно этапа холецистэктомии, недостоверно ниже исходного на 18,9 %, что позволяет говорить о восстановлении дооперационного уровня значений РИ.
Таблица 3.4.
Изменение показателей мозгового кровотока в контрольной и исследуемой группах (M m, * – p <0.05 – по сравнению с первым этапом)
|
Показатель |
Исх. |
Прем. |
Инт. |
Инсф. |
Хэкт. |
Кон. |
|
РИ К |
1,3042 |
1,1574 |
1,0132 |
0,9314 |
0,9717 |
1,0582 |
|
± 0,0959 |
± 0,0895 |
± 0,0960* |
± 0,1064* |
± 0,1064* |
± 0,1262 |
|
|
И |
1,2061 |
1,1601 |
1,1327 |
1,0439 |
0,9539 |
1,0011 |
|
± 0,1080 |
± 0,1061 |
± 0,1227 |
± 0,0863 |
± 0,0792 |
± 0,1010 |
|
|
АЧП К |
0,0157 |
0,0127 |
0,0101 |
0,0093 |
0,0100 |
0,0113 |
|
± 0,0012 |
± 0,0010 |
± 0,0010* |
± 0,0011* |
± 0,0011* |
± 0,0013* |
|
|
И |
0,0145 |
0,0135 |
0,0120 |
0,0112 |
0,0107 |
0,0114 |
|
± 0,0013 |
± 0,0013 |
± 0,0013 |
± 0,0009* |
± 0,0009* |
± 0,0011 |
|
|
ДкИ К |
0,7473 |
0,7289 |
0,7289 |
0,7016 |
0,7065 |
0,7089 |
|
± 0,0226 |
± 0,0181 |
± 0,0193 |
± 0,0228 |
± 0,0212 |
± 0,0174 |
|
|
И |
0,7089 |
0,6769 |
0,6365 |
0,6719 |
0,6499 |
0,6931 |
|
± 0,0233 |
± 0,0295 |
± 0,0332 |
± 0,0269 |
± 0,0229 |
± 0,0217 |
|
|
ДаИ К |
0,7490 |
0,7243 |
0,7245 |
0,7026 |
0,6772 |
0,6984 |
|
± 0,0224 |
± 0,0196 |
± 0,0200 |
± 0,0238 |
± 0,0190 |
± 0,0153 |
|
|
И |
0,7246 |
0,6812 |
0,6571 |
0,6770 |
0,6630 |
0,6979 |
|
± 0,0219 |
± 0,0311 |
± 0,0351 |
± 0,0265 |
± 0,0226 |
± 0,0215 |
После премедикации изменение АЧП не выражено значительно, однако отмечается снижение АЧП после интубации, инсуффляции и холецистэктомии соответственно на 33,5 %, 40,5 % и 35,8 % относительно первого этапа исследования, что свидетельствует о происходящем снижении объемного кровотока в ходе исследования. После операции также отмечается сниженный уровень АЧП на 27,9 %.
Изменения ДкИ и ДаИ менее выражены и статистически недостоверны, что позволяет говорить о стабильности этих показателей. Незначительная динамика диастолического и дикротического индексов показывает малое изменение тонуса сосудов мелкого и среднего калибра.
Характеризуя изменение параметров МК, следует отметить, что наибольшие изменения отмечаются на этапах интубации, инсуффляции и холецистэктомии, где уменьшение РИ существенное, происходит совместно с уменьшением АЧП, что говорит о снижении регионального кровотока в указанной зоне.

Рисунок 3.3. Изменение РИ и АЧП в контрольной и исследуемой группах (мозговой кровоток)
В исследуемой группе (табл. 3.4, рис 3), где проводилась дополнительная защита клофелином, изменение показателей регионального кровообращения было менее значимым. После премедикации отмечается снижение РИ лишь на 3,8 % относительно исходного уровня, изменение на этапах после интубации и инсуффляции также незначительны и составляют 6,1 % и 13,5 % соответственно. Наибольшее снижение РИ происходило на этапе холецистэктомии, однако оно также было недостоверным – меньше исходного значения на 20,9 %. В конце операции достоверного снижения РИ также не наблюдалось.
Значение АЧП в исследуемой группе остается неизменным после премедикации и интубации. После инсуффляции отмечается снижение АЧП на 22,3 % относительно исходного уровня и остается на этом уровне на этапе холецистэктомии – на 26,1 % ниже первого этапа. После операции происходит восстановление исходного уровня АЧП – недостоверно ниже на 21,1 %.
Изменение ДкИ и ДаИ в исследуемой группе не существенны. Отмечается некоторое незначительное снижение на этапах инсуффляции и холецистэкомии. Предел колебания ДкИ равен от 10,2 % на этапе интубации до 2,2 % в конце операции, ДаИ – от 9,3 % на этапе интубации до 3,7 % в конце операции.
Анализируя характер изменений в обеих группах следует отметить однонаправленность изменений РИ, однако в контрольной группе снижение РИ достоверное, чего не отмечено в исследуемой, менее выражено в процентном отношении и не подтверждается статистически
Важность изучения мозгового кровотока не вызывает сомнений, хотя МК в значительной степени регулируется механизмами авторегуляции, из которых следует отметить вазоконстрикторный и вазодилатационный. Отмечено, что верхней границей САД, при котором не предупреждается увеличения МК, является 150–170 мм.рт.ст. Нижняя граница, при которой происходит снижение МК, колеблется около 50–70 мм.рт.ст. На авторегуляцию МК влияют гиперкапния, гипоксия и ишемия, ставя, в критических ситуациях, его в полную зависимость от уровня артериального давления (Б.И. Шулутько, Ю.Л. Перов,1992).
В начало 3-й главы К содержанию монографии
3.2.2. Изменение параметров печеночного кровотока
Проведено исследование изменения основных параметров печеночного кровотока методом реографии (М.К. Осколкова, Г.А. Красина, 1980) у 15 пациентов контрольной группы, где проводилась общепринятая премедикация, и у 15 пациентов исследуемой группы, где в премедикацию дополнительно включали клофелин.
Исследование проводили на этапах:
- исходный, за сутки до операции, в палате;
- после премедикации на столе, до операции и индукции;
- после интубации, до начала операции;
- конец операции, после снятия пневмоперитонеума.
На этапах исследовали реографический индекс (РИ), амплитудно-частотный показатель (АЧП), дикротический (ДкИ) и диастолический индексы (ДаИ).
В контрольной группе (табл. 3.5, рис. 3.4) после премедикации наблюдается снижение РИ на 30,7 % относительно исходного уровня. Индукция, ларингоскопия и интубация трахеи вызывают снижение РИ на 51,3 %, значения РИ также ниже исходных и после операции – на 67,2 % относительно первого этапа исследований, что свидетельствует о снижении кровотока в бассейне воротной вены и печеночной артерии в предоперационном периоде, после интубации и после операции.
Таблица 3.5.
Изменение показателей печеночного кровотока в контрольной и исследуемой группах (M m, * – p<0.05 – по сравнению с первым этапом)
|
Показатель |
Исх. |
Прем. |
Инт. |
Кон. |
|
РИ К |
1,1125 |
0,7708 |
0,5417 |
0,3646 |
|
± 0,1270 |
± 0,1074* |
± 0,0595* |
± 0,0349* |
|
|
И |
1,1500 |
0,8375 |
0,6000 |
0,5125 |
|
± 0,1785 |
± 0,1432 |
± 0,0486* |
± 0,0631* |
|
|
АЧП К |
0,0134 |
0,0085 |
0,0054 |
0,0039 |
|
± 0,0015 |
± 0,0012* |
± 0,0006* |
± 0,0004* |
|
|
И |
0,0138 |
0,0101 |
0,0066 |
0,0062 |
|
± 0,0021 |
± 0,0017 |
± 0,0005* |
± 0,0008* |
|
|
ДкИ К |
0,6500 |
0,6812 |
0,6417 |
0,5250 |
|
± 0,0160 |
± 0,0343 |
± 0,0367 |
± 0,0473 |
|
|
И |
0,6040 |
0,6473 |
0,6321 |
0,5767 |
|
± 0,0678 |
± 0,0334 |
± 0,0367 |
± 0,0263 |
|
|
ДаИ К |
0,6205 |
0,6853 |
0,6417 |
0,5250 |
|
± 0,0294 |
± 0,0436 |
± 0,0392 |
± 0,0473 |
|
|
И |
0,5811 |
0,6353 |
0,5929 |
0,5967 |
|
± 0,0693 |
± 0,0270 |
± 0,0404 |
± 0,0346 |
Изменение объемного кровотока также значимо. После премедикации происходит снижение АЧП на 36,5 %, после интубации АЧП ниже на 59,4 %, еще более снижаясь в конце операции – на 70,9 % в сравнении с исходным уровнем.
Изменение ДкИ и ДаИ говорит об некотором повышении сосудистого тонуса после премедикации, некотором снижении после интубации (относительно этапа премедикации). Большее снижение отмечается в конце операции, однако все эти изменения происходят недостоверно, что не позволяет говорить об колебании сосудистого тонуса на указанных этапах.
В исследуемой группе (табл. 3.5, рис. 3.4) после премедикации снижения РИ не наблюдается, его изменение недостоверно. После интубации снижение РИ есть, на 47,8 % относительно исходных значений. В конце операции значение РИ также ниже на 55,4 %, однако, в сравнении с контрольной группой менее выражено.

Рисунок 3.4. Изменение РИ и АЧП в контрольной и исследуемой группах (печеночный кровоток)
Изменение объемного кровотока после премедикации не отмечается, но после интубации наблюдается снижение АЧП на 52,2 %, в конце операции – на 55,4 %.
Изменение показателей ДкИ и ДаИ в исследуемой группе также недостоверно, повторяет направленность изменений контрольной группы и не характеризует значимое изменение сосудистого тонуса.
Сравнивая изменение параметров ПК следует сказать, что в контрольной группе снижение показателей РИ и АЧП происходит уже после премедикации, еще более снижаясь после интубации и в конце операции. В исследуемой группе после премедикации снижения РИ и АЧП не наблюдается. Отмечается снижение РИ и АЧП после интубации, в конце операции, но если в контрольной группе снижение на этих этапах происходит почти в два раза, то в исследуемой существенно меньше, что подтверждает указанный процент изменения этих параметров.
Тенденция изменений показателей тонуса сосудов (ДкИ и ДаИ) не подтверждает значимых сдвигов как в контрольной, так и в исследуемой группах. Следует отметить однонаправленность изменений сосудистого тонуса в обеих группах, но на основании малого процента изменения указанных показателей и данных статистического анализа следует говорить о стабильности этих параметров ПК.
Кровоток в спланхническом бассейне при вмешательствах на верхнем этаже брюшной полости влияет на течение послеоперационного периода, результат проведенного вмешательства, активность репаративных процессов. Оценка печеночного кровотока как одного из важных спланхнических регионов особенно значима. Возможное существенное снижение печеночного кровотока при стрессорных воздействиях не вызывает сомнений. Но в данном случае «спланхническая зона» является и зоной «хирургического интереса», что затрудняет исследование кровотока неинвазивными методами при использовании закрытой техники холецистэктомии, делает невозможным использование всех доступных инвазивных методик. В связи с этим нами проведена оценка состояния печеночного кровотока в ответ на некоторые основные стрессорные воздействия в ближайшем послеоперационном периоде.
Изменение регионального кровообращения в ответ на стрессорное воздействие также следует рассматривать как механизм адаптации к новым условиям существования, стрессорному воздействию. Также следует учитывать тот факт, что если системный кровоток может поддерживаться на вполне достаточном уровне, то нарушения регионального кровотока могут быть более выраженными и, тем не менее, это в меньшей степени учитывается в клинической практике. Вместе с тем нарушения именно этого звена циркуляции крови могут вести к снижению обеспечения тканей необходимыми для жизнедеятельности ресурсами и, в итоге, вести к нарушению функции органов, систем. Известно, что уменьшение сердечного выброса, повышение периферического сопротивления могут привести к нарушению регионального кровотока, иногда выраженному, что может сопровождаться появлением симптомов ишемии органов. (Е.И. Чазов, 1992). Опасность декомпенсации в случаях с повышенным риском вмешательства требует внимания как к оценке функционального резерва организма, так и ставит вопрос о необходимости постоянного клинического наблюдения за состоянием пациента во время вмешательства.
Таким образом, в ответ на проводимое вмешательство отмечаются реакции регионального кровотока головного мозга и печени в обеих группах. Включение клофелина в премедикацию позволило создать условия для обеспечения стабильности МК. В исследуемой группе отмечается меньшее изменение показателей РИ и АЧП на этапах исследования, стабильность значений в конце операции.
При использовании клофелина отмечается меньшая динамика показателей ПК, меньшее снижение в конце операции показателей РИ и АЧП, что свидетельствует об эффективности использования клофелина с целью дополнительной антистрессорной защиты и коррекции регионарного кровотока.
В начало 3-й главы К содержанию монографии
3.3. Изменения центральной и периферической гемодинамики у больных в операционном и ближайшем послеоперационном периодах при применении АЗК и АГЛ
Одной из актуальных проблем анестезиологии является изыскание способов предупреждения и устранения нарушений кровообращения у оперированных больных. Оперативные вмешательства на органах брюшной полости, как правило, травматичны и продолжительны, часто сопровождаются значительной кровопотерей. Это может вызвать выраженные расстройства микроциркуляции, системной и органной гемодинамики, снижение ОЦК (Б.Р. Гельфанд, В.А. Новожилов, 1977; И.П. Назаров, Г.И. Лещак, 1989).
Несмотря на значительный прогресс современной анестезиологии, проблема предупреждения нарушений гемодинамики у оперированных больных еще далека от своего решения. Одним из перспективных направлений в решении этой задачи следует считать предупреждение излишних реакций симпато-адреналовой системы и надпочечников в ответ на операционную травму. Торможение нейроэндокринной системы предупреждает рефлекторные нарушения кровообращения и развитие операционного и травматического шока (Н.В. Лян, А.А. Тогайбаев, 1970; В.П. Гадалов, 1985; Е.А. Вагнер с соавт., 1986). Изучение состояния микроциркуляции и периферического кровообращения представляется целесообразным, т. к. по мнению ряда авторов (Т.П. Тулбуре с соавт., 1985; Н.П. Александрова, 1987) изменение микроциркуляции является наиболее ранней реакцией организма на стрессорные воздействия, в т.ч. операцию и кровопотерю.
В данном разделе мы сделали попытку ответить на вопрос о возможности предупреждения и коррекции нарушений центральной гемодинамики и микроциркуляции применением АЗК и АГП у больных, оперированных на органах брюшной полости.
В начало 3-й главы К содержанию монографии
3.3.1. Изменение параметров гемодинамики и микроциркуляции у больных с исходной артериальной нормотонией
У больных контрольной группы (табл. 3.6, рис. 3.5) еще до операции, несмотря на проведение премедикации, происходило достоверное учащение пульса и повышение САД, что мы связываем с дооперационным стрессом и введением атропина перед операцией. В дальнейшем на протяжении всего операционного периода и в раннем послеоперационном периоде удерживалась тахикардия более 100 уд/мин. САД до операции и в течение всего операционного периода, за исключением травматичного этапа, было достоверно выше исходной величины на 9–11 %. В различные этапы операционного периода УИ сердца уменьшался на 17–18 %, возвращаясь к исходному лишь через 1 час после операции, а СИ поддерживался на цифрах не ниже исходного в течение всей операции за счет тахикардии, достоверно увеличиваясь на 15,9–16,1 % в раннем послеоперационном периоде.
На протяжении всего периода исследования, за исключением травматичного этапа операции отмечено достоверное увеличение МРЛЖ по сравнению с исходной величиной на 14,7–27,5 %. Потребность миокарда в кислороде (ПМО2) у больных данной группы возрастала после доставки в операционную на 27 % и оставалась достоверно выше на 24,6–46,2 % исходной величины на протяжении всего исследования. Изменения ПСС были статистически не существенны.
Одновременное уменьшение УИ при увеличении МРЛЖ и ПМО2 может свидетельствовать о снижении сократительной способности миокарда и увеличении нагрузки на сердце.
При анализе показателей объемного пульса и кожно-фарингиального температурного градиента (табл. 3.9, рис. 3.6) у больных контрольной группы после доставки в операционную отмечено достоверное, по сравнению с нормой, снижение амплитуды пульсовой волны на 49 %, суммы внутренних радиусов сосудов на 52 %, объемного кровотока на 49 % и минутного кровотока пальца на 38 %.

Рисунок 3.5. Изменение пульса, САД и УИ у больных с исходной артериальной нормотонией
Таблица 3.6.
Показатели центральной гемодинамики у больных контрольной группы с исходной артериальной нормотонией (М m; n = 40).
|
Показатели гемодинамики |
Периоды исследования |
||||||
|
исх. |
д/о |
п/и |
т/э |
к/р |
п/э |
ч/ч |
|
|
Пульс, |
82.2 ± 1.46 |
97.7 ± 3.87 <0.001 |
101.0 ± 2.19 <0.001 |
103.9 ± 1.90 <0.001 |
106.0 ± 2.30 <0.001 |
110.9 ± 2.11 <0.001 |
101.6 ± 2.71 <0.001 |
|
АДс, |
128.0 ± 2.01 |
137.0 ± 2.56 <0.02 |
140.9 ± 4.95 <0.02 |
126.2 ± 3.30 >0.5 |
142.1 ± 3.71 <0.01 |
138.7 ± 2.80 <0.02 |
130.0 ± 2.62 >0.5 |
|
АДд, |
80.5 ± 2.5 |
89.0 ± 1.47 <0.01 |
94.3 ± 3.30 <0.001 |
85.3 ± 1.69 >0.1 |
91.7 ± 1.92 <0.001 |
89.9 ± 2.30 <0.01 |
82.4 ± 1.61 >0.5 |
|
САД, |
96.3 ± 2.55 |
105.0 ± 1.84 <0.01 |
109.8 ± 3.83 <0.001 |
98.9 ± 2.31 >0,5 |
108.5 ± 2.09 <0.001 |
106.2 ± 2.49 <0.02 |
98.3 ± 2.60 >0.25 |
|
УИ, Р1 |
46.8 ± 1.2 |
42.6 ± 1.67 >0.05 |
38.3 ± 1.54 <0/001 |
39.3 ± 2/07 <0.01 |
39.8 ± 1.81 <0.01 |
40.1 ± 1.96 <0.01 |
43.9 ± 1.43 >0.1 |
|
СИ, |
3.84 ± 0.14 |
4.16 ± 0.21 >0.1 |
3.87 ± 0.25 >0.5 |
4.08 ± 0.20 >0.25 |
4.22 ± 0.24 >0.1 |
4.4 ± 0.21 <0.02 |
4.46 ± 0.18 <0.01 |
|
МРЛЖ, |
8.62 ± 0.26 |
10.17 ± 0.34 <0.001 |
9.87 ± 0.38 <0.01 |
9.39 ± 0.32 >0.05 |
10.65 0.52 <0.001 |
10.99 ± 0.62 <0.001 |
10.20 0.36 <0.001 |
|
ПСС, |
1170 ± 84 |
1179 ± 90 >0.5 |
1326 ± 77 >0.2 |
1132 ± 64 >0.5 |
1201 ± 62 >0.5 |
1115 ± 57 >0.5 |
1030 ± 75 >0.1 |
|
ПМО2, |
10522 ± 286 |
13385 ± 560 <0.001 |
14231 ± 656 <0.001 |
13112 ± 584 <0.001 |
15063 ± 615 <0.001 |
15382 ± 602 <0.001 |
13208 ± 505 <0.001 |
Р1 – достоверность с исходным.
* здесь и далее: исх – исходное; д/о – до операции после премедикации; п/и – после интрубации; т/э – травматичный этап; к/о – конец операции; п/э – после экстубации; ч/ч – через 1 час.
Таблица 3.7.
Показатели центральной гемодинамики у больных с применением АЗК в группе с исходной артериальной нормотонией (М m; n = 40)
|
Показатели гемодинамики |
Периоды исследования |
||||||
|
исх. |
д/о |
п/и |
т/э |
к/р |
п/э |
ч/ч |
|
|
Пульс, Р2 |
82.9 ± 2.18 >0.5 |
83.2 ± 1.91 >0.5 <0.001 |
84.6 ± 1.97 >0.5 <0.001 |
78.2 ± 2.03 >0.1 <0.001 |
78.0 ± 2.03 >0.05 <0.001 |
85.3 ± 2.16 >0.25 <0.001 |
86.5 ± 2.04 >0.1 <0.001 |
|
АДс, Р1 Р2 |
130.8 ± 2.56 |
125.0 ± 3.12 >0.1 <0.01 |
126.1 ± 3.19 >0.1 <0.02 |
118.0 ± 3.08 <0,002 >0.05 |
120.2 ± 2.96 <0.01 <0.001 |
122.3 ± 3.74 >0.05 <0.001 |
123.9 ± 3.97 >0.1 >0.1 |
|
АДд, Р2 |
80.6 ± 1.96 >0.5 |
79.2 ± 1.84 >0.05 <0.001 |
80.4 ± 1.18 >0.5 <0.001 |
73.0 ± 1.38 <0.002 <0.001 |
77.8 ± 1.54 >0.25 <0.001 |
78.5 ± 1.76 >0.25 <0.001 |
79.3 ± 1.92 >0.5 >0.1 |
|
САД, Р2 |
97.3 ± 2.26 >0.5 |
94.5 ± 2.58 >0.25 <0.001 |
95.6 ± 2.31 >0.5 <0.002 |
88.0 ± 2.43 <0.01 <0.002 |
91.9 ± 2.25 >0.05 <0.001 |
93.1 ± 2.94 >0.25 <0.001 |
94.2 ± 3.04 >0.25 >0.25 |
|
УИ, Р1 Р2 |
46.4 ± 1.31 >0.5 |
46.0±1.44 >0.5 >0.1 |
48.6 ± 1.89 >0.25 <0.001 |
49.1 ± 1.53 >0.1 <0.001 |
48.7 ± 1.60 >0.25 <0.001 |
47.4 ± 1.46 >0.5 <0.01 |
47.1 ± 2.03 >0.5 >0.1 |
|
СИ, Р2 |
3.85 ± 0.19 >0.5 |
3.83 ± 0.13 >0.5 >0.1 |
4.11 ± 0.22 >0.25 >0.25 |
3.84 ± 0.27 >0.5 >0.25 |
3.80 ± 0.29 >0.5 >0.25 |
4.05 ± 0.21 >0.25 >0.1 |
4.08 ± 0.24 >0.25 >0.1 |
|
МРЛЖ, Р2 |
8.72 ± 0.30 >0.5 |
8.42 ± 0.26 >0.25 <0.001 |
9.15 ± 0.32 >0.25 >0.1 |
7.89 ± 0.28 <0.05 <0.001 |
8.12 ± 0.35 >0.1 <0.001 |
8.77 ± 0.29 >0.5 <0.002 |
8.94 ± 0.40 >0.5 <0.05 |
|
ПСС, Р2 |
1180 ± 114 >0.5 |
1153 ± 116 >0.5 >0.5 |
1085 ± 122 >0.5 >0.05 |
1067 ± 98 >0.25 >0.5 |
1130 ± 106 >0.5 >0.5 |
1074 ± 136 >0.5 >0.5 |
1079 ± 149 >0.5 >0.5 |
|
ПМО2, Р2 |
10843 ± 389 >0.5 |
10400 ± 511 >0.25 <0.001 |
10668 ± 483 >0.5 <0.001 |
9228 ± 443 <0.01 <0.001 |
9376 ± 490 <0.02 <0.001 |
10432 ± 382 >0.25 <0.001 |
10717 ± 361 >0.5 <0.001 |
Р1 – достоверность с исходным.
Р2 – достоверность с контролем.
Таблица 3.8.
Показатели центральной гемодинамики у больных с применением АГП в группе с исходной артериальной нормотонией (М m; n = 40)
|
Показатели гемодинамики |
Периоды исследования |
||||||
|
исх. |
д/о |
п/и |
т/э |
к/р |
п/э |
ч/ч |
|
|
Пульс, Р2 Р3 |
82.0 ± 2.46 >0.5 >0.5 |
80.8 ± 1.92 >0.5 <0.001 >0.25 |
83.8 ± 1.71 >0.5 <0.001 >0.5 |
81.9 ± 2.06 >0.5 <0.001 >0.1 |
80.1 ± 1.44 >0.25 <0.001 >0.25 |
81.4 ± 2.09 >0.05 <0.001 >0.1 |
86.3 ± 2.78 >0.1 <0.001 >0.5 |
|
АДс, Р1 Р2 Р3 |
131.2 ± 2.68 >0.25 >0.5 |
122.7 ± 2.14 <0.02 <0.001 >0.5 |
119.4 ± 4.82 <0.05 <0.001 >0.1 |
116.4 ± 3.42 <0,001 <0.05 >0.5 |
124.6 ± 4.42 >0.1 <0.01 >0.25 |
132.3 ± 4.00 >0.5 >0.1 >0.05 |
135.8 ± 3.86 >0.25 >0.1 <0.05 |
|
АДд, Р2 Р3 |
83.8 ± 1.61 >0.25 >0.1 |
78.1 ± 1.61 <0.02 <0.001 >0.5 |
74.6 ± 2.14 <0.001 <0.001 <0.02 |
73.9 ± 2.29 <0.001 <0.001 >0.5 |
81.5 ± 3.04 >0.5 <0.01 >0.25 |
85.0 ± 3.38 >0.5 >0.1 >0.05 |
83.9 ± 2.14 >0.5 >0.5 >0.1 |
|
САД, Р2 Р3 |
99.6 ± 1.98 >0.25 >0.25 |
93.0 ± 1.61 <0.02 <0.001 >0.5 |
89.5 ± 2.42 <0.01 <0.001 >0.05 |
88.1 ± 2.23 <0.001 <0.001 >0.5 |
95.9 ± 3.50 >0.25 <0.002 >0.25 |
100.8 ± 3.40 >0.5 >0.1 >0.05 |
101.0 ± 2.10 >0.5 >0.25 >0.05 |
|
УИ, Р1 Р2 Р3 |
46.3 ± 1.08 >0.5 >0.5 |
47.3±1.61 >0.5 <0.05 >0.5 |
49.2 ± 1.63 >0.1 <0.001 >0.5 |
49.2 ± 1.39 >0.05 <0.001 >0.5 |
45.9 ± 1.99 >0.5 <0.05 >0.25 |
46.0 ± 1.76 >0.5 <0.05 >0.5 |
48.0 ± 2.04 >0.25 >0.05 >0.5 |
|
СИ, Р2 Р3 |
3.79 ± 0.12 >0.5 >0.5 |
3.82 ± 0.16 >0.5 >0.1 >0.5 |
4.12 ± 0.15 >0.05 >0.25 >0.5 |
4.03 ± 0.20 >0.25 >0.5 >0.5 |
3.67 ± 0.23 >0.5 >0.05 >0.5 |
3.74 ± 0.28 >0.5 <0.05 >0.25 |
4.14 ± 0.30 >0.25 >0.25 >0.5 |
|
МРЛЖ, Р2 Р3 |
8.79 ± 0.18 >0.5 >0.5 |
8.27 ± 0.26 >0.05 <0.001 >0.5 |
8.59 ± 0.28 >0.5 >0.01 >0.1 |
8.27 ± 0.26 <0.05 <0.01 >0.25 |
8.20 ± 0.22 >0.05 <0.001 >0.5 |
8.78 ± 0.33 >0.5 <0.01 >0.5 |
9.74 ± 0.41 >0.05 <0.25 >0.1 |
|
ПСС, Р2 Р3 |
1227 ± 103 >0.5 >0.5 |
1136 ± 94 >0.5 >0.5 >0.5 |
1013 ± 106 >0.1 >0.02 >0.5 |
1020 ± 128 >0.1 >0.25 >0.5 |
1218 ± 111 >0.5 >0.5 >0.5 |
1257 ± 137 >0.5 >0.25 >0.25 |
1138 ± 168 >0.5 >0.5 >0.5 |
|
ПМО2, Р2 Р3 |
10758 ± 475 >0.5 >0.5 |
9914 ± 353 >0.1 <0.001 >0.25 |
10006 ± 520 >0.25 <0.001 >0.25 |
9533 ± 397 <0.05 <0.001 >0.5 |
9980 ± 387 <0.1 <0.001 >0.25 |
10769 ± 386 >0.5 <0.01 >0.5 |
11720 ± 666 >0.1 <0.05 >0.05 |
Р1 – достоверность с исходным .Р2 – достоверность с контролем Р3 – достоверность между исследуемыми группами.
Таблица 3.9.
Изменение показателей объемного пульса и кожно-фарингиального температурного градиента у больных с исходной нормотонией (M±m; n = 20)
|
Показатель |
Группы больных |
Норма |
Периоды исследования |
|||
|
д/о |
т/э |
к/о |
ч/ч |
|||
|
h, мм |
К Р1 АЗК Р1 Р2 АГП Р1 Р2 Р3 |
7.0±0.30 |
3.6±0.23 <0.002 7.1±0.43 >0.5 <0.001 7.4±0.38 >0.5 <0.001 >0.5 |
5.8±0.37 >0.5 9.5±0.51 <0.05 <0.001 10.3±0.56 <0.01 <0.001 >0.25 |
5.0±0.35 >0.05 8.9±0.47 >0.05 <0.001 9.3±0.52 <0.05 <0.001 >0.5 |
3.8±0.42 <0.01 8.0±0.48 >0.25 <0/001 8.6±0.50 >0.1 <0.001 >0.25 |
|
Ео |
К Р1 АЗК Р1 Р2 АГП Р1 Р2 Р3 |
5.7±0.50 |
13.3±0.65 <0.001 6.5±0.32 >0.1 <0.001 6.0±0.37 >0.5 <0.001 >0.25 |
7.1±0.61 >0.05 4.7±0.42 >0.1 <0.01 41±0.41 <0.05 <0.001 >0.25 |
10.1±0.47 <0.001 4.8±0.34 >0.01 <0.001 4.6±0.34 <0.05 <0.001 >0.5 |
12.5±0.51 <0.001 5.6±0.47 >0.1 <0.001 6.0±0.43 >0.5 <0.001 >0.5 |
|
Vо |
К Р1 АЗК Р1 Р2 АГП Р1 Р2 Р3 |
14.0±1.10 |
6.7±1.15 <0.001 12.2±1.05 >0.1 <0.01 13.0±1.02 >0.5 <0.001 >0.5 |
12.0±0.82 >0.1 15.5±1.12 >0.25 <0.05 18.0±1.26 <0.05 <0.001 >0.1 |
9.1±0.77 <0.002 16.2±0.96 >0.1 <0.001 17.7±1.19 <0.05 <0.001 >0.25 |
6.6±1.09 <0.001 13.2±1.23 >0.5 <0.001 13.9±1.31 >0.5 <0.001 >0.5 |
|
S, мм2 |
К Р1 АЗК Р1 Р2 АГП Р1 Р2 Р3 |
64.0±3.25 |
32.5±3.44 <0.001 62.8±4.61 >0.5 <0.001 68.4±4.54 >0.25 <0.001 >0.25 |
38.7±2.96 <0.001 88.1±4.93 <0.001 <0.001 90.5±5.11 <0.001 <0.001 >0.5 |
35.3±3.82 <0.001 85.7±5.08 <0.002 <0.001 86.6±4.84 <0.001 <0.001 >0.5 |
28.6±4.11 <0.001 73.4±4.56 >0.1 <0.001 77.9±5.01 <0.05 <0.001 >0.5 |
|
МКП, мм2/мин |
К Р1 АЗК Р1 Р2 АГП Р1 Р2 Р3 |
5120±265 |
3175±224 <0.001 5225±237 >0.5 <0.001 5227±230 >0.5 <0.001 >0.5 |
4021±221 <0.01 6889±234 <0.001 <0.001 7412±268 <0.001 <0.001 >0.1 |
3741±235 <0.001 6685±294 <0.001 <0.001 6937±253 <0.001 <0.001 >0.5 |
2906±351 <0.001 6349±321 <0.01 <0.001 6723±370 <0.01 <0.001 >0.25 |
|
D t |
К Р1 АЗК Р1 Р2 АГП Р1 Р2 Р3 |
2.5±0.30 |
5.0±0.36 <0.001 2.6±0.31 >0.5 <0.001 2.0±0.37 >0.2 <0.001 >0.1 |
4.2±0.28 <0.001 1.6±0.22 <0.05 <0.001 1.4±0.25 <0.02 <0.001 >0.5 |
4.6±0.31 <0.001 1.8±0.27 >0.05 <0.001 1.4±0.31 <0.02 <0.001 >0.25 |
5.2±0.42 <0.001 2.4±0.35 >0.5 <0.001 2.4±0.35 >0.5 <0.001 >0.5 |
Р1 – достоверность с исходным. Р2 – достоверность с контролем, Р3 – достоверность между исследуемыми группами
с одновременным увеличением модуля упругости на 133 % и температурного градиента на 100 %. Эти изменения свидетельствовали о резком повышении тонуса сосудов и снижении периферического кровотока с ухудшением микроциркуляции под влиянием основного заболевания и психо-эмоционального напряжения перед операцией.
Во время операции отмечалось увеличение амплитуды пульсовой волны, суммы внутренних радиусов сосудов и снижение модуля упругости по сравнению с дооперационными величинами. Однако на протяжении всей операции и в ближайшем послеоперационном периоде оставались достоверно сниженными минутный кровоток пальца (на 21,5–43,2 %) и объемный кровоток (на 40–55,3 %) при увеличении температурного градиента (на 68–108 %). Эти изменения говорят о плохом состоянии микроциркуляции у больных контрольной группы до операции, во время операции и в ближайшем послеоперационном периоде, несмотря на статистически не существенные изменения ПСС.
У больных с применением АЗК (табл. 3.7, рис. 3.5) частота пульса после премедикации и на протяжении всей операции практически не отличалась от исходной. УИ и СИ несколько увеличивались в травматичный этап, однако эти сдвиги были статистически не существенными. Наряду с этим, МРЛЖ достоверно уменьшалась на 10 %, а ПМО2 в травматичный этап и в конце операции снижалась на 14–15 %. Эти изменения свидетельствовали об увеличении эффективности работы сердца с одновременным уменьшением нагрузки на него. ПСС в течение всего периода наблюдения существенно не изменялось.
Изменения гемодинамики у больных на фоне АГП представлены в табл. 3.8 и на рис. 3.5. Применение адрено- и ганглиолитиков вызывало сходные с клофелином изменения гемодинамики. Отмечена стабилизация пульса на уровне, близком к исходному, на всех этапах исследования. Изменения УИ, СИ, МРЛЖ, ПСС и ПМО2 также имели сходный с АЗК характер. Особенно следует отметить, что применение АЗК и АГП не вызывало гипотонию, САД максимально снижалось на 10 % и 11,6 % соответственно. Показатели УИ уже после премедикации и в течение всей операции были достоверно выше (на 11–28,5 %), СИ существенно не отличался, а МРЛЖ ниже (на 13,5–30 %),чем у больных контрольной группы. На этом фоне отмечено значительное, по сравнению с контрольной группой, снижение ПМО2 (на 35–50,9 %).

Рисунок 3.6. Изменение Ео и Vо у больных с исходной нормотонией
При анализе показателей объемного пульса и кожно-фарингиального температурного градиента (табл. 3.9, рис. 3.6) в группах с применением АЗК и АГП уже после премедикации отмечена нормализация всех исследованных показателей. На всех этапах исследования микроциркуляция была достоверно лучше, чем у больных контрольной группы. Существенных различий между группами с применением АЗК и АГП отмечено не было.
Таким образом, проведенные исследования свидетельствуют о высокой эффективности применения АЗК и АГП с целью предупреждения неблагоприятных сдвигов центральной гемодинамики и нарушений микроциркуляции у больных с исходной нормотонией под влиянием дооперационного стресса, операции и анестезии.